|
アルギニン(NO)
は、テロメラーゼおよび長寿遺伝子(サーチュイン)を活性化し、寿命を延ばし、老化および老化病を抑制し、若返りが期待できる超画期的成分です!! (レスベラトロールやTA-65よりすごい!?アルギニン)
|
||
1.老化はどうして起こるか、老化はどうすれば防げるか 老化はどうして起こるか -現在最も有力な老化の原因説と長寿・若返りのための対策法- -120歳以上の長寿と20代への若返りも夢ではない- 1)遺伝子説とは 1-1)テロメア説 1-1-1)ストレスによるテロメア短縮とその抑制 a)抗酸化成分の血中濃度とテロメアの長さとの関係 b)微量栄養素(ビタミン、ミネラルなど)はテロメアの長さにどう影響するか c)栄養素とテロメアの関係(レビュー) d)運動とテロメアの関係 1-1-2)テロメラーゼとその活性化 a)テロメラーゼの再活性化によって若返ることができる!! b)食生活とテロメラーゼ活性の関係 c)体内成分とテロメラーゼとの関係 ◎ビタミンDとテロメラーゼの関係 ◎女性ホルモンとテロメラーゼの関係 ◎アルギニン(NO)とテロメラーゼの関係 1-1-3)アルギニン(NO)および他成分のテロメラーゼおよびテロメアに対する作用と 老化および老化病抑制作用(まとめ) 図.アルギニン(NO)および他成分のテロメラーゼおよびテロメアに対する作用と 老化および老化病抑制作用との関係 【その他のテロメア長維持物質(特にTA-65について)】 1-2)長寿遺伝子説 1-2-1)ミトコンドリアとは 1-2-2)ミトコンドリアと老化および老化病、肥満、メタボリックシンドロームとの関係 a)ミトコンドリアと老化および老化病 b)ミトコンドリアと肥満 c)ミトコンドリアとメタボリックシンドローム 1-2-3)ミトコンドリアとアルギニン 【その他のサーチュイン活性化物質(特にレスベラトロールについて)】 2)摩耗説とは 3)老化対策について 2.アルギニンの寿命延長、老化および老化病の予防・改善作用 1)アルギニンの寿命延長作用 2)アルギニンの老化および老化病の予防・改善効果 表.アルギニン(NO)の寿命延長、抗老化、老化病抑制作用 図.アルギニン(NO)の寿命延長、抗老化および老化病抑制のメカニズム 3.お知らせ(ホームページ責任者、参考図書) |
| 【お問合せ先】 本ページおよびアルギニンに関するお問い合わせは本ページ責任者古賀までお願いします (Eメール:kogahrs555@nifty.com) ★上記以外のアルギニンの働きについてお知りになりたい方は 『アンチエイジングで若返る!』をご覧ください。 |
 1.老化はどうして起こるか、老化はどうすれば防げるか 1.老化はどうして起こるか、老化はどうすれば防げるか
次に、老化説(若返り説)としての遺伝子説と摩耗説についてより詳しく述べます。 1)遺伝子説とは 遺伝子説とは、寿命や老化は遺伝子に組み込まれているとするものです。動物の寿命は種によって固有の寿命があります。例えば、人の最大寿命は約120歳で、マウスの最大寿命は3歳以下です。このような種による寿命の違いは遺伝的に決まっています。また、身体の老化現象の多く、例えば、しわ、白髪、薄毛、物忘れなどのほとんどは程度の差はあれ加齢に伴って必然的に出現し、丁度遺伝的にそれぞれがプログラムされているように見えます。また、女性の閉経は、一定の年齢になると全ての女性に起こり、遺伝的にプログラムされています。このように、寿命や老化は遺伝的にプログラム化されているという説をプログラム説と言い、その主体がテロメア説です。 一方、遺伝子の中には、それを活性化することで、長寿と老化予防と若返りをもたらすことができる遺伝子があるとする説を長寿遺伝子説と言います。長寿遺伝子として現在最も注目されているものにサーチュイン遺伝子があります。 1-1)テロメア説 テロメア説については、テロメアとテロメラーゼの発見に寄与した3人の科学者に、2009年ノーベル生理学・医学賞が授与されたことで一躍有名になり、マスコミなどに広く取り上げられるようになって、それらに働く成分がさも若返りや長寿の夢の特効薬のように言われたことがあります。このところ世間的にはそのブームも少し覚めた感じがありますが、実際には医学や科学の世界では次々とそれを裏付けるデータも蓄積されてきています。そこで、最新のデータも含め、それを医学的、科学的に検証してみたいと思います。 また、アルギニン(NO)はテロメラーゼを活性化し、テロメア長を維持しますが、アルギニンが寿命(生存率)や老化や老化病にどういう働きを示すかについても述べたいと思います。 生物の設計図であるDNAは、例えば私たち人の細胞では46本に分けられ、それぞれ線状の染色体として存在しています。この染色体の末端についているのがテロメアです。テロメアの働きは、一つは染色体末端の保護、もう一つは染色体の末端を完全に複製することです。ところで、テロメアには避けがたい宿命があります。それは細胞分裂に伴ってDNAが複製されるたびに短くなることです。人のテロメアは最初1万~2万塩基対ありますが、細胞が増殖する過程で、1回の細胞分裂あたり100~150塩基対ほど短くなります。テロメアが5000塩基対位まで短くなると細胞は分裂を停止し、細胞は老化しやがて死んでしまいます。このように、組織や臓器に老化細胞が増えていくと、組織や臓器は縮小し、働きも低下し身体全体が老化し人は死んでしまいます。ところで、人の最大寿命は120歳程度と考えられていますが、テロメアの長さから計算した最大寿命とほぼ一致します。ではどうしてほとんどの人は120歳前に死亡するのでしょうか。それは、人のテロメアは長い人と短い人がいるということです(個人差が大きい)。60歳あたりからすでに平均テロメア長が5000塩基対程度になる人もいれば、100歳になっても十分に長いテロメアを持っている人もいます。実際、テロメアが長い人と短い人を比べた場合、テロメアが短い人より長い人の方が長生きするというデータがあります。テロメアが短かった人たちは心臓血管系(3.18倍の死亡率増加)や感染症(8.54倍の死亡率増加)で亡くなる頻度が高かったそうです5,6)。なお疫学研究において、短い白血球のテロメア長(全身のテロメアの長さを反映)と、より高い死亡率、老化の促進および慢性疾患(老化病)(肥満、高脂血症、動脈硬化、心血管病、心不全、2型糖尿病、高血圧、骨粗鬆症など)のより高いリスクとが関連することが報告されています。このことは、テロメアが短くなると老化が促進され、肥満、高脂血症、動脈硬化、心血管病、心不全、2型糖尿病、高血圧、骨粗鬆症などの慢性疾患(老化病)や感染症に罹りやすくなり、死亡率が高くなるものと考えられます。そのため、若さや健康を保つためにはテロメアを長く保つことは極めて重要なこととなります。 【注】最近、慶応大学医学部が、英国のニューカッスル大学との共同研究によって、百寿者(100歳以上)や遺伝的に百歳に到達する確率が高いと考えられる百寿者の直系子孫(血縁のある子供)では、テロメア長がより長く保たれており、実際の年齢が80歳代でも、60歳代の平均値に匹敵する長さを有していることが分かったことを報告しています(百寿者の秘訣:健康寿命を延ばす二つの要因を発見 -1,554 名を対象とする大規模高齢者コホート研究-)。 1-1-1)ストレスによるテロメア短縮とその抑制 しかしながら、最初同じくらいのテロメア長を持っていても寿命は同じとは限りません。それは、テロメアは色々なストレスによっても短くなるということです。ストレスとして、放射線、紫外線や活性酸素などがありますが、これらはゲノムを損傷しテロメアを短縮します。中でも活性酸素によってゲノムは日常的に損傷しテロメアを短縮します〔放射線や紫外線を体に浴びると体内で活性酸素(フリーラジカル)が生成しますが、これが放射線や紫外線による体の傷害の主な原因となります〕。そのため、活性酸素に対し有効な対策を取ることは、テロメア短縮を遅らせ老化を防ぐのに有効と考えられています。 a)抗酸化成分の血中濃度とテロメアの長さとの関係 実際、抗酸化成分の血中濃度とテロメアの長さとの関係を調べた研究があります7)。平均年齢66歳の高齢者(男女786人、オーストリア)について、ビタミンC、ルテイン、ゼアキサンチン、β-クリプトキサンチン、カンタキサンチン、リコペン、ビタミンE、カロテン、レチノールの血中濃度と白血球のテロメアの長さ(全身のテロメアの長さを反映)が測定されました。その結果、ルテイン、ゼアキサンチンおよびビタミンCとテロメア長との間に明らかに正の相関関係がありました。中でもビタミンCが最も相関関係が強力でした。一方、その他の抗酸化成分はテロメア長と相関関係はありませんでした。このことは抗酸化成分、中でも特にビタミンンCがテロメアの長さの維持に保護的効果を有することを示しています。 b)微量栄養素(ビタミン、ミネラルなど)はテロメアの長さにどう影響するか また、一方、女性(586人。年齢35~74歳。米国)についての疫学研究において、微量栄養素(ビタミン、ミネラルなど)が白血球のテロメア長にどう影響するかが調べられました8)。被験者の65%がマルチビタミン(色んなビタミンやミネラルを万遍なく配合)を摂取していました。そのうち74%がほぼ毎日摂取していました。マルチビタミンを毎日摂取している人は、摂取していない人に比べ、平均5.1%長いテロメアを有していました。この差は約9.8年分のテロメアに相当します。このことは、マルチビタミンを毎日摂取している人は、摂取していない人に比べ、生物学的に約10年若いということになります。この効果は抗酸化剤サプリメント(抗酸化成分を主に配合)でも同様に認められました。このことは、マルチビタミンや抗酸化成分がストレス(活性酸素など)を抑制することでテロメアの短縮を防いだためと考えられます。さらに、食物から摂取した微量栄養素がテロメア長にどういう影響があるかが検討されました。その結果、ビタミンCとビタミンEをより多く摂取している人では明らかに(統計的に有意に)長いテロメアを有していることが示されました。一方、他の微量栄養素はテロメア長と関係ありませんでした。マルチビタミンを摂取していないグループでもビタミンCとビタミンEのより多い摂取はより長いテロメアと関係していました。これらの結果は、ビタミンや抗酸化成分、特にビタミンCは、テロメアの短縮を抑制し、生存率(寿命)を伸ばし、老化を抑制し、慢性疾患(老化病)(動脈硬化、2型糖尿病、高血圧、肥満など)のリスクを低減させることが期待できることを示しています。〔実際、Khawらによれば(Lancet, 357, 657 (2001))、ビタミンCは、全死亡率、心血管病、虚血性心疾患、がんによる死亡率を最大約1/3まで減少させることが報告されています〕。 c)栄養素とテロメアの関係(レビュー) 栄養素とテロメアの関係をまとめた文献があります9)。テロメアの長さは加齢、ストレス、感染症、肥満、慢性病(特に老化病、例えば、メタボリックシンドローム、生活習慣病、アルツハイマー病、パーキンソン病、がんなど)によって短くなることが知られています。加齢の場合は細胞分裂を繰り返したため、ストレス、感染症、慢性病の場合はそれらによって障害を受け消失した細胞を補うために細胞分裂が増加したため、テロメアが短縮していきます。これらの病気の根底には炎症が関与しています。炎症は酸化ストレスを生じます。そのため、炎症や酸化ストレスを軽減する成分はテロメアの短縮を防ぐことができます。テロメアは、健康的なライフスタイルや食事で長く維持されます。また、テロメアの長さを長くするテロメラーゼ(後述)の活性にもライフスタイルや食事が影響することが知られています。この文献では食事の成分(栄養素)がテロメアの長さにどう影響するかについて述べています。 ●葉酸(ビタミンB群の一つ)はテロメアの合成に必要ですので、それが不足するとテロメアが短くなります。また、葉酸は体内で還元体になりますが、それが抗酸化作用を示します。加えて、葉酸は、活性酸素を生成し、動脈硬化を引き起こすホモシステインを低下させます。このように、葉酸はその活性酸素抑制作用によってテロメアを活性酸素の害から保護している可能性があります。 ●ビタミンB12をサプリメントとして摂取すると、摂取しない場合に比べテロメアが長く維持されることが報告されています(女性)。ビタミンB12は抗酸化活性と抗炎症作用を持っています。そのため、高用量をサプリメントとして摂取した場合、ビタミンB12の抗酸化作用と抗炎症作用がテロメアを長く維持するのに寄与したものと考えられます。 ●ニコチンアミド(ナイアシン)(ビタミンB群の一つ)は細胞においてテロメアの短縮を抑制します。ニコチンアミドは活性酸素の生成を抑制します。 ●ビタミンAとβ-カロテンは、食事から摂取した場合、テロメア長を長く維持します(女性)。ビタミンAとβ-カロテンの抗酸化活性がテロメア長の維持に寄与したものと考えられます。なお、ビタミンAとβ-カロテンはサプリメントとして摂取した時、死亡リスクを増加させる可能性があるという報告があります10)。また、ビタミンAの過剰摂取は様々な安全性面での問題を生じます11)。β-カロテンの過剰症は特に報告されていませんが、喫煙者(過去喫煙していた人も含め)がサプリメントとしてβ-カロテンを摂取した場合、肺がん、前立腺がん、脳出血、心臓血管病、および死亡のリスクが増加する可能性があります12)。これらのことから、ビタミンAとβ-カロテンは食事から摂ることをおすすめします。サプリメントとして摂ることはおすすめできません。 ●ビタミンDの血中濃度と白血球のテロメア長との間に正の相関関係があることが報告されています(女性)。ビタミンDは抗炎症作用を示しますのでこれがテロメアの短縮を防いでいるものと考えられます。 ●ビタミンCとビタミンEは良く知られていますように、抗酸化活性を持っています。ビタミンCとビタミンEは、食事として摂取した場合でも、サプリメントとして摂取した場合でも、摂取量に応じてテロメアがより長くなりました(女性)。細胞を用いた試験において、ビタミンCとビタミンEは、通常の場合に比べ、細胞の寿命を数倍伸ばしました。また、細胞の老化を抑制しました。加齢に伴うテロメアの短縮はビタミンCとビタミンEで半分近くまで抑制されました。加齢に伴うテロメラーゼ活性の低下もビタミンCとビタミンEで抑制されました。このことは、活性酸素を消去することによって、活性酸素によるテロメアの短縮とテロメラーゼの活性低下が抑制され、テロメア長を長く保つことで寿命が伸び、老化が抑制されることを示しています。 ●マグネシウムは、食事として摂取した場合、テロメア長を長く維持します(女性)。マグネシウムが欠乏した状態を続けると、酸化ストレスが増加し、テロメアは短くなります(ラット、細胞)。 ●亜鉛は、テロメラーゼ活性を高めます。高齢者において、テロメアの短縮が限界に達した細胞(細胞分裂できない老化した細胞)の割合や、テロメア長の短縮の程度は、細胞内の亜鉛の減少の程度と関係していました。亜鉛は酸化ストレスを減少させます。このように、亜鉛は酸化ストレスの軽減やテロメラーゼ活性の増加などによってテロメア長に影響する可能性があります。 ●鉄は、他の栄養成分と異なり、テロメアを短くします。鉄は活性酸素を生成させ酸化ストレスを増加させます。鉄によるテロメアの短縮は、鉄による活性酸素の生成と酸化ストレスの上昇によるものと考えられます。そのため、病気の治療のために必要な場合を除き、鉄の摂りすぎは控えるべきと考えられます。 ●オメガ-3脂肪酸(ドコサヘキサエン酸、エイコサペンタエン酸)の血中濃度とテロメア短縮の軽減の大きさの間に正の相関関係があることが示されています。オメガ-3脂肪酸の血中濃度と、低レベル炎症マーカーと高レベル抗炎症マーカーとが相関していました。また、オメガ-3脂肪酸の摂取は、抗酸化酵素(スーパーオキシドディスムターゼ、カタラーゼ、グルタチオンペルオキシダーゼ)の活性を増強し、寿命を延長しました(マウス)。オメガ-3脂肪酸による抗炎症活性と抗酸化活性が細胞のターンオーバーとDNAの酸化的障害を減少させ、その結果テロメアの短縮を抑制したものと考えられます。 ●ブドウ種子とお茶に含まれるポリフェノールは抗炎症活性と抗酸化活性を持つことが報告されています。実際、お茶を習慣的に飲む人は、たまにしか飲まない人に比べ、長いテロメアを有していました(約5年の生存期間の差に相当)。また、ブドウ種子ポリフェノールの摂取はより長いテロメアと相関する傾向が見られました(マウス)。 ●ウコンの成分クルクミンはポリフェノールの一種です。クルクミンは抗酸化活性と抗炎症活性を示します。クルクミンを摂取させたとき、DNAの障害が減少し、テロメアの長さがより長く維持される傾向がありました(マウス)。 ●抗酸化栄養素として知られているコエンザイムQ10もテロメアを長く維持することが報告されています(ラット)13)。通常のラットおよび酸化ストレスが増加したラットを用いて検討されました。通常のラットにコエンザイムQ10を摂取させると、長いテロメアの割合が増加しました。一方、短いテロメアの割合は減少しました。酸化ストレスの増加したラットでは長いテロメアの割合は通常のラットに比べ減少し、一方、短いテロメアの割合は増加していましたが、コエンザイムQ10を摂取させると、長い部分と短い部分のテロメアの割合はそれぞれ通常ラットのレベルまで回復しました。これは、コエンザイムQ10の抗酸化作用によって、活性酸素によるテロメアの酸化障害が抑制され、テロメア長が長く維持されたものと考えられました。 d)運動とテロメアの関係 一方、ライフスタイルの改善がテロメアを長くすることが知られています。運動は、肥満、高血圧、高脂血症、糖尿病、動脈硬化、アルツハイマー病、骨粗鬆症、がんなどの代謝異常(メタボリックシンドローム)や慢性病を予防・改善し、死亡率を低下させ、健康に良いことは良く知られています。これらの異常や病気は老化と関係があると考えらえています。そのため、運動はテロメアの短縮を抑制する可能性があります。これらを背景に運動とテロメアの長さとの関係を検討した研究があります14)。双子の男女2401人(女性2152人、男性249人。年齢18~81歳。英国)が試験に採用されました。試験者の白血球のテロメアの長さは個人間でかなり差があり、4.9から9.1キロベース(kb)の範囲でした(平均7.0kb)。テロメアの長さは年齢とともに短くなり、年間の平均消失数は21.0ヌクレオチド(b)でした。運動レベルは4段階に分類されました〔運動習慣なし(余暇時間における1週間当たりの平均運動時間16分)、短い運動時間(同36分)、中程度の運動時間(同102分)、長い運動時間(同199分)〕。肥満度(BMI)の増加は運動レベルの減少およびより短いテロメア長と有意に相関していました。余暇時間の運動レベルと平均テロメア長との関係では、運動レベルが増加するにつれて明らかに(統計的に有意に)テロメアが長くなりました。運動習慣なしグループに比べ、長い運動時間グループのテロメアは平均200ヌクレオチド(b)長いことが示されました。この差は9.5年分のテロメアに相当します。このことは、良く運動する人は、運動しない人に比べ、生物学的に約10年若いということになります。これらの結果は、運動による老化や老化病の抑制、あるいは死亡率の低下などの健康効果の少なくとも一部は、運動によるテロメア長の維持効果が関わっているということを示しています。では、運動がどうしてテロメア長の維持効果を示すのでしょうか。適度な運動は体内の抗酸化ストレス能を高めることが知られています。これは運動による酸化ストレスの増加に対抗するために体内の抗酸化システム(抗酸化酵素など)が増強されるためではないかと考えられています(これを運動ホルミシス現象と言います)15)。 では、健康に良い運動とはどのようなものでしょうか。これに対する検討結果が報告されています16)。運動習慣のない健康な人を、3種類の強度の運動に分けました。弱い強度の運動群〔25%VO2max(最大酸素摂取量の25%の強度)〕、中等度の強度の運動群(50%VO2max)、強い強度の運動群(75%VO2max)です。各強度群の被験者は自転車エルゴメーターを使って、1日30分間、週5~7回、12週間、各強度の運動を行いました。運動の健康効果は、アセチルコリン刺激による前腕血流量の増加(血管内皮細胞の働きに異常があるかどうかの指標の一つ。内皮細胞の機能に異常があると、動脈硬化や心血管病を起こすリスクが高くなります。糖尿病、高血圧症などの患者で一般的にみられます。血管内皮細胞からのNOの生成量の増加と関係があります。NOは血管を拡張し、動脈硬化を防ぎます)を指標としました。その結果、中等度の強度の運動群では、アセチルコリン刺激による前腕血流量の増加は50%増強されました。一方、弱い強度の運動群と高い強度の運動群では、アセチルコリン刺激による前腕血流量の増加の増強は見られませんでした。つまり、最大酸素摂取量の半分(50%)の中等度の運動では、運動による健康効果が見られたのに対し、最大酸素摂取量の25%の弱い強度の運動と最大酸素摂取量の75%の高い強度の運動では、運動による健康効果が見られなかったということです。弱い強度の運動では運動の強さが弱いために運動による健康効果がでなかったものと納得できますが、強い強度の運動の場合どうして運動による健康効果が出なかったのでしょう。これを明らかにするために、強い強度の運動の場合の、体内の酸化ストレス(活性酸素)に対する影響が検討されました。その結果、強い強度の運動の場合、体内の酸化ストレスは明らかに(統計的に有意に)上昇しました。一方、弱い強度の運動の場合、体内の酸化ストレスは変化ありませんでした。中等度の運動の場合、体内の酸化ストレスはかえって弱くなる傾向が見られました。このことは、中等度の強度の運動では、運動によって生成した活性酸素は、その刺激によって誘導された抗酸化酵素によって完全に消去され、さらにその抗酸化酵素は元々体内にある活性酸素の一部までも消去したと考えられるのに対し、強い強度の運動では、運動によって生成した活性酸素の量が多すぎて、誘導された抗酸化酵素だけではそれを消去することができなかったため、体内の抗酸化ストレスが上昇したものと考えられます。従って、運動習慣のない健康な人が、健康を維持するため、あるいは病気のリスクを回避するために運動する場合、おすすめする最適な運動の強度は、最大酸素摂取量の半分(50%)位です。運動の強度は弱すぎても効果がないし、強すぎては酸化ストレスによる障害によって病気に罹りやすくなり、寿命も短くなるでしょう。 では、運動とマルチビタミン(抗酸化ビタミンを含んでいます)や抗酸化サプリメントを併用すれば、それぞれの効果が発揮されて、テロメア長はさらに長く維持されるでしょうか。事はそんなに簡単ではないようです。運動と抗酸化サプリメント(ビタミンC+ビタミンE)を併用した場合、抗酸化サプリメントは運動の健康効果を打ち消すことが報告されました17)。ではどうしてそういうことが起こったのでしょうか。適度な運動は適度に活性酸素の産生量を増やします。これによってPGC1α/β、PPARγが誘導されます。PGC1α/βは、体内の抗酸化酵素(スーパーオキシドジスムターゼ(SOD)、グルタチオンペルオキシダーゼ(GPX1)、カタラーゼ)を誘導するとともに、種々の健康効果、例えば、インシュリン感受性の向上などをもたらします。ところが、運動と抗酸化サプリメントを併用すると、運動によって生じた活性酸素が抗酸化サプリメントによって消去されました。それとともに、PGC1α/β、PPARγの誘導はほぼ完全に抑制され、SOD、GPX1などの抗酸化酵素の誘導もほぼ完全に抑制されました。また、種々の健康効果も消失しました。運動と抗酸化サプリメント(やマルチビタミン(抗酸化ビタミンが含まれています))を併用すれば相加的あるいは相乗的な効果が得られるのではないかと考えていた私たちにとってこれらのデータは衝撃的でした。 以上のデータから、運動とマルチビタミンや抗酸化サプリメントが、お互いのテロメア維持効果や健康効果になるべく影響しないで最大限の効果を発揮するようにするには、例えば、運動習慣のない人ではマルチビタミンや抗酸化サプリメントを毎日摂取することがテロメア長の維持や健康を保つには重要と考えられます。一方、運動習慣のある人では運動日はマルチビタミンや抗酸化サプリメントの摂取は止めたほうがよいでしょう。運動日でない日は摂取したほうがよいと思われます。ただ、激しい運動をする人は活性酸素の発生が体内の抗酸化システムの能力を上回り、酸化障害を起こす可能性がありますのでマルチビタミンや抗酸化サプリメントの積極的な摂取をおすすめします。抗酸化成分としてビタミンEを用いる場合はその摂取量に気を付けてください。ビタミンEは1日に150IU(100mg)を超えた量を摂取すると死亡率が増えるというメタアナリシスの結果が報告されています18)。この理由として、大量のビタミンEが存在すると、ビタミンEと活性酸素が反応して生成するビタミンEラジカルの量が増え、これがプロオキシダント(酸化促進物質)となって傷害を引き起こすためと考えられています。そのため、おすすめするビタミンEの摂取量は1日150IU(100mg)以下です。それを超えた量ですと長期間の摂取で死亡率が増加する可能性があります。 1-1-2)テロメラーゼとその活性化 一方、テロメアはテロメラーゼという酵素によって伸ばすことができます。テロメラーゼは人では生殖細胞や幹細胞(多能性幹細胞)に高い活性が検出されますが、その他の体細胞のほとんどに活性が認められません。ただ、組織幹細胞〔皮膚や血液や肝臓のようなきまった組織や臓器で、消失したり死滅したりして細胞が足りなくなった時それを補うために新しい細胞を作り続けている幹細胞。例えば、骨髄には造血幹細胞があり赤血球や白血球などの血液細胞を作っています。また、皮膚や肝臓では細胞が次々と作られたり再生するのも、骨折が治るのも、髪の毛が伸びるのもこの組織幹細胞の働き(自己複製能)のおかげです。現在、神経、上皮、心筋、肝、消化管上皮、生殖、造血、間葉系、骨格筋など様々な場所に見つかっています〕には弱いテロメラーゼ活性が発現していて、細胞分裂ごとのテロメア短縮を抑制し一生を通じて多くの細胞を供給できますが、テロメラーゼ活性が弱く、年齢とともに徐々にテロメアが短縮し、結局細胞は老化します。このことは、これら組織幹細胞に見られるテロメラーゼ活性は、テロメア短縮による細胞老化を防ぐことができないほど不十分であり、機能細胞を供給し続けられないということです。また、細胞の老化とともにテロメラーゼ活性が低下するとの報告もあります。これらのことから、組織幹細胞の弱いテロメラーゼ活性をより強くすることで、老化防止や若返り、はては120歳以上の長寿を達成しようという試みが盛んにおこなわれています。他方、テロメラーゼはがん細胞の多くに高い活性が示され、それががん細胞に無限増殖性を与えていることが考えられます。しかしながら、最近の研究で、テロメラーゼの活性化だけでは細胞はがん化(造腫瘍性)しないことが示されていますが、完全にその懸念を払拭するまでには至っていません6)。そのため、現在は、テロメラーゼ活性を自在に発現調節できる方法や成分の開発が試みられています。 a)テロメラーゼの再活性化によって若返ることができる!! テロメラーゼの活性化が若返りの特効薬になりうる可能性を示した研究があります19)。ハーバード大学医学部のJaskelioffらが行った研究で、テロメラーゼ活性を失くしたマウスでは、機能障害を起こした短いテロメアを示し、細胞は5~6回の継代培養後分裂を停止し、老化した細胞の形態を示しました。つまり細胞はほとんど分裂しない静止状態になりました。また、DNA損傷の増加、種々の組織の機能低下、特に増殖性の高い組織、例えば生殖細胞のアポトーシスによる極度の精巣萎縮と睾丸サイズの減少とそれによる生殖能力の低下、顕著な脾臓の機能低下、クリプト細胞のアポトーシスに伴う腸陰窩の減少と絨毛の退化、脳における神経幹細胞の自己複製能の減少や神経細胞増殖能の低下などによる脳重量の減少、嗅覚減退など老化したマウスに見られる現象が見られました。また、テロメラーゼの活性を失くしたマウスではそうでないマウスに比べ寿命がほぼ半分に短縮しました。一方、このマウスの細胞にテロメラーゼが再活性化されるような処置を行うと、テロメアは長くなり、細胞は分裂増殖を再開し、さらに8回以上の継代培養後も分裂し続けました。さらにこのマウスではテロメラーゼ再活性化後わずか4週間後に、組織や臓器の若返りが見られました。精巣の生殖細胞のアポトーシスの減少による正常な精巣サイズへの回復と生殖能力の増加、脾臓重量の回復、腸クリプト細胞のアポトーシスの減少が見られました。また、脳においては神経幹細胞の自己複製能の回復や神経細胞増殖能の正常化、脳重量の回復などが見られました。嗅覚に関してはほぼ正常レベルまで回復しました。このマウスでは寿命も延長しました。 人の典型的な老化現象には、白髪、皮膚の弾力の低下としわ、視力の低下、聴力の低下、嗅覚の低下、筋力の低下、骨折しやすくなる、血管の老化(動脈硬化など)、性機能の低下、記憶力の低下などが見られますが、これらはほとんどがテロメアの短縮による組織幹細胞の機能低下が原因で、新しい細胞が供給されにくくなったためと考えられます。Jaskelioffらによる上記研究では、テロメラーゼ活性の消失によるテロメアの短縮により増殖停止状態(老化状態)にある組織幹細胞が、テロメラーゼの再活性化によりテロメア長を回復し、増殖能を回復して、細胞や組織や臓器の若返りが起こったものと考えられます。このことから、人においても、テロメラーゼの活性化によるテロメアの伸長や、ストレスなどによるテロメア短縮の抑制などによりテロメア長を長く保つことができれば、120歳以上の長寿や、本当の意味での若返り(細胞、組織、臓器および身体全体の若返り)が可能になるのではないかと考えられます。 では、人の場合、テロメラーゼはどうすれば活性化できるのでしょうか。人では遺伝子工学的にテロメラーゼを活性化することは現在のところほとんど不可能ですし、がん化の危険もあります。そのため、生体物質や人間が昔から摂取してきてがん化の危険がない物質を摂取することでテロメラーゼを活性化できれば理想的です。実はそのような物質がいくつか見出されてきています。そのような物質をうまく摂取することで長寿や若返りができたらすごく素敵ですしワクワクしますよね!一方、ライフスタイルを工夫することでもテロメラーゼが活性化されることが知られています。 b)食生活とテロメラーゼ活性の関係 先ず、ライフスタイルがテロメラーゼにどういう影響を及ぼすかについて見てみましょう。食事の違いが健康や寿命に大きくかかわることは良く知られています。日本食が健康に良く、日本人の長寿命に寄与しているとか言われています。一方、地中海食の健康効果もよく知られています。地中海食は健康に最も良い食事の一つと言われています。10年間の追跡調査によって、地中海食をよく食べる人は、そうでない人に比べ、死亡率が低く、心血管病やがんによる死亡率が低下しました20)。また、脂質代謝、血管拡張性、糖質代謝、抗酸化ストレス能など心血管病の危険因子に対して良い効果を示します。さらに、地中海食はより長い寿命と健康寿命をもたらすことが示されています。また、細胞を酸化ストレスから守り、細胞の老化や細胞死(アポトーシス)を防ぎ、テロメアの短縮を抑制することが示されました。 ではどの程度地中海食を食べればテロメア長の維持や健康効果に結び付くのでしょうか。さらに地中海食はテロメラーゼの活性に影響するのでしょうか。これらを明らかにするため検討がなされました21)。217人の白人(イタリア住人)の男女(平均年齢77.9歳)が試験に登録されました。白血球のテロメアの長さは年齢とともに減少しました。1年年を取るごとにテロメアは58塩基(b)だけ短くなりました。年齢とは関係なく、女性のほうが男性より長いテロメアを持っていました。その差は330bでしたので、女性は男性より生物学的に5.7年若いということになります。なお、イタリア人の平均寿命(2012年)は男性80歳、女性85歳ですので22)、テロメアの長さの差から計算した年齢差とほぼ一致しました。このことから、テロメアの長さを測ることによって余命を調べることができるかもしれません。実際、テロメアの長さを測って余命を推測しようという試みはすでに色々行われています23)。次に、喫煙とテロメアの関係が調べられました。そうしますと、喫煙者では、非喫煙者に比べ、テロメアは490b短縮していました。これは、喫煙者は非喫煙者に比べ8.4年生物学的に老化しているということになります。ところが過去喫煙歴があっても禁煙することによってテロメアは長く維持されることが示されました(喫煙歴があるが現在喫煙していない人では、非喫煙者と比べ、テロメアは60b短かっただけでした)。白血球のテロメアの長さとテロメラーゼ(PBMC)活性との間には有意な正の関係がありました。このことは、テロメアの長さの少なくとも一部はテロメラーゼの働きによるものと言えます。 被験者は、地中海食をどの程度摂取したかによって分類されました。分類は地中海食スコア(MDS)に従って3分類に分けました。第一分類は低スコア群(MDSが3以下)、第二分類は中スコア群(MDSが4~5)、第三分類は高スコア群(MDSが6以上)です。MDSとは、食物群を9分類し、男女別の摂取量の中央値を計算し、各食物群の摂取量が中央値より多いか少ないかでスコア化したものです。有益と考えられる食物群(野菜、マメ科植物、果実、穀物、魚、一価不飽和脂肪/飽和脂肪比)の摂取量や比が中央値より多い場合1のスコアを、少ない場合0のスコアを、有害と考えられる食物群(魚肉以外の肉、乳製品)の摂取量が中央値より少ない場合1のスコアを、多い場合0のスコアを与えました。アルコールにつきましては、スコア1が、男性の場合1日摂取量が10~50g(エタノールとして)の時、女性の場合1日摂取量が5~25g(エタノールとして)の時与えられました。このようにMDSの合計は0~9となります。MDSが0の人は地中海食をほとんど実行しない人で、9の人は地中海食を忠実に実行する人です。(MDSについては詳しくは文献24を参照ください)。 MDSの各スコア群とテロメアの長さやテロメラーゼ活性との関係を調べてみますと、高スコア群のテロメアの長さやテロメラーゼ活性は(統計的に)有意に低スコア群や中スコア群よりも高値でした。テロメアは加齢によって短縮しますが、地中海食はこの短縮をどれくらい抑制できるのでしょうか。MDS低スコア群、中スコア群、高スコア群の1年間のテロメアの短縮数は、それぞれ72b、57b、51bでした。つまり、地中海食をほとんど実行しない人と地中海食を忠実に実行する人とでは、1年間にテロメアの長さが21b違ってくるということになります。10年間では210bになるとしますと、地中海食をよく食べる人はそうでない人に比べ、10年経った時生物学的に3.6年(平均の年間テロメア短縮数58で割った時)若いということになります。(また別の計算では、両者の最初のテロメア長が各10000bだったとして、これが5000bまで短くなると、細胞は分裂を停止し老化し死滅(アポトーシス)するとしますと、地中海食をほとんど実行しない人では69年で老化してやがて死んでしまいますが、地中海食を忠実に実行する人では老化するまでには98年かかるということになります。実に29年もの差ができてしまうことになります。個体レベルで、実際にここまで差が出るかどうかはわかりませんが、疫学的研究は地中海食がより長い寿命と健康寿命をもたらすことを示しています)。また、テロメラーゼは地中海食をよく食べる人ではより活性化されますが、MDS低スコア群に比べ高スコア群ではテロメラーゼ活性は約20%活性化されていました。 では、地中海食の何がテロメア長やテロメラーゼ活性に影響しているのでしょうか。MDS高スコア群の人たちの炎症性成分や活性酸素由来成分の血中濃度は、低スコア群に比べ低値を示しました。テロメアの長さやテロメラーゼ活性は、炎症スコアや活性酸素由来成分と負の相関関係がありました。炎症スコアは活性酸素由来成分と正の相関関係にありました。このことは、炎症反応が活性酸素の生成を高め、テロメアやテロメラーゼを障害し、テロメアの短縮やテロメラーゼ活性の低下を引き起こしているものと考えられました。一方、地中海食は炎症を抑え、活性酸素の生成を抑制することで、テロメアの短縮やテロメラーゼ活性の低下を抑制するものと考えられました。 次に、MDSスコアと健康度がどう相関するかについて見てみますと、健康な高齢者(高血圧、心筋梗塞、血管病、認知症、脳卒中、心不全を持たない人)の比率はMDSスコアが大きくなるほど高くなり、低スコア群に比べ高スコア群で1.6倍でした(健康な人の割合は低スコア群で34.3%、高スコア群で54.4%)。また、健康な高齢者のテロメアは、不健康な高齢者(上記の病気の二つ以上を併発)より長く(220bの差)、テロメラーゼ活性も健康な高齢者のほうがより高活性でした。 以上をまとめてみますと、地中海食、すなわち、野菜、マメ科植物、果実、穀物、魚、オリーブオイル(一価不飽和脂肪酸を豊富に含みます)を積極的に摂取し、魚肉以外の肉や乳製品の摂取をできるだけ控え、アルコールはほどほど(男性では1日にワインにして約90ml~450ml、女性では1日にワインにして約45~225mlが適正量です。但し、これはイタリアの白人の場合です。日本人の場合再検討する必要があるかもしれません25)。)にした食事は、脂質代謝、血管拡張性、糖質代謝の異常など心血管病のリスクを低下させ、心血管病やがんによる死亡率を低下させ、より長い寿命と健康寿命をもたらします。この地中海食の健康効果は、主にその抗炎症効果および抗酸化活性に由来するものと考えられます。この抗炎症活性と抗酸化活性がテロメアを長くし、テロメラーゼ活性を高めたものと考えられます。一方、テロメラーゼはテロメアを長くします。つまり、地中海食は、その抗炎症活性と抗酸化活性によって、直接テロメアの障害を抑制して、テロメア長を長く維持し、また、その抗炎症活性と抗酸化活性によって(地中海食に含まれる栄養成分によって直接テロメラーゼが活性化される可能性もありますが)テロメラーゼ活性を高めることで間接的にテロメアを長くするものと考えられました。この長く維持されたテロメアによって、地中海食をよく食べる人に見られる、種々の健康効果と健康寿命の延長と長寿がもたらされたものと考えられます。 c)体内成分とテロメラーゼとの関係 ◎ビタミンDとテロメラーゼの関係 ビタミンDは、腸管でのカルシウムの吸収を促進し、骨の形成を助けるビタミンとして知られていますが、そのほかに様々な作用を持っています。例えば、筋肉、炎症、免疫系、心血管系、脳神経系などへの作用が報告されています。ビタミンDはその作用機構と機能の多様性からホルモンに分類されることもあります。ビタミンDの欠乏は、種々の老化性疾患、例えば、骨粗鬆症、筋力低下、高血圧、2型糖尿病、心血管病、死亡率と関係があります。また、ビタミンDの体内濃度の低下は、種々の自己免疫疾患(多発性硬化症、関節リウマチ、1型糖尿病など)のリスク増大と関係がありました。一方、ビタミンDの摂取は、骨粗鬆症や筋力低下を改善し、血管の硬さや内皮反応性(動脈硬化と関係)を改善し、免疫関連疾患(1型糖尿病、多発性硬化症、関節リウマチ)の発症を抑制し重症度を減弱しました。ビタミンDの体内濃度と炎症マーカー(CRP)の間に逆の相関がみられ、ビタミンDは炎症反応を抑制すると考えられました。ビタミンDは脳神経系にも影響を与えます。ビタミンDの欠乏は認知機能の低下を引き起こし、認知症やアルツハイマー病のリスクを増大させました(ビタミンDが欠乏した人たちは、ビタミンDが欠乏していない人たちに比べ、認知症やアルツハイマー病発症のリスクが2倍以上増加しました)26)。一方、ビタミンDの摂取は、老化による学習能力や記憶力の低下を改善しました。高齢者においてはビタミンDの体内濃度は低下しますので、これらの疾患のリスクはより増大するものと考えられます。そのため、特に高齢者ではサプリメントなどによりビタミンD(特に日光による活性化が必要でないビタミンD3)の積極的な摂取がすすめられます〔しかし、摂りすぎは過剰症(高カルシウム血症、腎障害など)を引き起こしますのでご注意ください。成人のビタミンDの1日の摂取量目安は5.5μgです。上限量は50μg/日です。海外品には大量のビタミンDが含まれているものがありますのでご注意ください〕。これらのビタミンDの作用にはテロメアやテロメラーゼが関与している可能性が考えられました。 2160人の女性(平均年齢49.4歳、英国)について、ビタミンD(25-ヒドロキシビタミンD)体内濃度と白血球テロメア長との関係が検討されました27)。加齢によって白血球のテロメアは短縮しました。年間のテロメアの短縮数は21.5bpでした。25-ヒドロキシビタミンD濃度とテロメア長との間には正の相関がみられました。炎症マーカー(CRP)の濃度とテロメア長および25-ヒドロキシビタミンDの濃度との間には負の関係が見られました。被験者たちを25-ヒドロキシビタミンDの濃度に応じて3つに分類したところ、濃度が高いほどテロメア長は長くなりました。濃度が最も低い人たちのテロメア長と濃度が最も高い人たちのテロメア長の差は107.1bpでした。つまり、25-ヒドロキシビタミンD濃度が最も高い人たちは最も低い人たちに比べ生物学的に5年若いということになります(5年長生きする可能性があります)。被験者の約1/3(700人)がビタミンDのサプリメントを摂取していたために、ビタミンD摂取とテロメア長との関係が調べられました。ビタミンDを摂取している人たちは摂取していない人たちに比べより長いテロメア長を有していました。その差は110bpでした。このように、ビタミンDの濃度が高い人たちは低い人たちに比べより長い白血球のテロメア長を有していました。また、ビタミンDのサプリメントからの摂取によってもテロメア長は長く維持されることが明らかにされました。ビタミンDのこの作用は、炎症を抑制することで活性酸素の生成を抑え、それによるテロメアの障害を抑制し、それによってテロメア長が長く維持されたものと考えられました。ビタミンDによるテロメア長の維持によって生物学的老化が5年ほど抑制されると考えられました。 ビタミンDによるテロメア長の維持にテロメラーゼが関係しているかが検討されました28)。肥満したアフリカ系アメリカ人は通常ビタミンDが不足していますので、その人たちを被験者としました。試験はランダム化二重盲検プラセボ対照臨床試験で行われました。被験者はビタミンD〔~2,000IU(~50μg)/日〕を摂取させたグループ(19人)とプラセボ(偽薬)群(18人)にランダムに分けられました。試験は16週間行われました。ビタミンDを摂取させたグループでは、摂取前に比べテロメラーゼ活性(PBMC)は19.2%増加していました。プラセボグループのテロメラーゼ活性(PBMC)は試験前に比べ変化はありませんでした。ビタミンDの血中濃度増加の程度とテロメラーゼ活性の増加の程度との間には有意な相関がありました。上記しましたように、ビタミンDはテロメア長を長く維持しますが、その働きの少なくとも一部はビタミンDのテロメラーゼ活性増加作用が関与しているものと考えられました。 ◎女性ホルモンとテロメラーゼの関係 女性は男性に比べ長生きです。日本人の平均寿命は女性が86.6歳で、男性は80.2歳です(2013年厚生労働省調査)。また、100歳以上の高齢者数は58,820人(平成26年。厚生労働省調査)で、そのうち女性の占める割合は87.1%です。寿命における性差はテロメアに関係があると考えられています。生まれたばかりの頃はテロメアの長さに性差はありません。しかし、その後、男性のテロメア長は女性に比べ早く短くなります。短いテロメアは老化や老化病(心血管病、認知症、糖尿病、肝硬変、潰瘍性大腸炎、腎不全など)と関係があるといわれていますが、実際、これらの疾患の中には男性が罹りやすいものが多いようです(心血管病、脳血管性痴呆、糖尿病、肝硬変など)。また、男性の短いテロメアが寿命の短さと関係があるといわれています29)。実際、ある報告によると、年齢とは関係なく、女性のほうが男性より長いテロメアを持っていました(被験者はイタリアの平均年齢77.9歳の男女)。テロメア長の差から計算した時、女性は男性より生物学的に5.7年若いということになりました。なお、この差は平均寿命の差〔約5年。男性の平均寿命80歳、女性の平均寿命85歳(2012年)〕22)とほぼ一致しました。 では、テロメア長における男女の差は何が原因なのでしょうか。その大きな要因の一つが女性ホルモンです。テロメアは活性酸素によって傷つけられやすく、それによってテロメアは短くなります。そのため、テロメアの長さを維持するためには活性酸素の害からテロメアを守ってやる必要があります。エストロゲン(女性ホルモン)は活性酸素の生成を抑えます。一方、テストステロン(男性ホルモン)はそのような作用を持っていません。この差が男女におけるテロメア長の差の原因の一つになっている可能性があります。 テロメア長の維持にはテロメラーゼの働きが極めて重要です。テロメラーゼは短くなったテロメアも長くすることができます。そのためテロメラーゼの活性化はテロメアを長く保ち、老化や老化病を防ぎ寿命の延長ももたらします。エストロゲンは直接あるいは間接的にテロメラーゼを活性化します29)。なお、エストロゲンによるテロメラーゼの活性化には、eNOS(血管内皮型一酸化窒素合成酵素)の活性化によるNO(一酸化窒素)の生成が必要なことが報告されています30)。 このように、生殖期にある女性ではエストロゲンによる酸化ストレスの軽減作用やテロメラーゼ活性化作用によりテロメアが長く維持されるため、女性は男性に比べ老化や老化病に罹りにくいですが、閉経後はエストロゲンの急激な低下により、その保護作用がなくなり、その後は男性と同様に老化や老化病が進みますが31)、生殖期での貯金があるため(女性では男性に比べ長いテロメアを持っているため)、結果的に、男性に比べて女性では老化や老化病発症の遅延や長寿命がもたらされるものと考えられます。 内因性のエストロゲンとテロメアの関係が検討されました32)。女性においては、生殖期年数、つまり、内因性のエストロゲンによる曝露年数(初潮から閉経までの期間として計算)の長さと老化や老化病(心血管病、認知症など)に対するリスクの低下が関係すると考えられています。そこで、閉経後の女性を対象に、内因性のエストロゲンの曝露年数とテロメア長やテロメラーゼ活性との関係が検討されました。53人の閉経後の女性(全員がホルモン療法を受けていました)が被験者となりました。内因性のエストロゲンの曝露年数の長さとテロメアの長さ、および低下したテロメラーゼ活性との間に有意な(統計的に)関係がありました。つまり、生殖期年数が長いほどテロメアも長くなり、逆にテロメラーゼ活性は低下するということを示しています。一方、閉経後のホルモン療法の長さとテロメア長やテロメラーゼ活性との関係は見出されませんでした。このことから内因性のエストロゲンは女性において細胞老化の抑制と関係があると考えられました。本研究では、内因性のエストロゲンの曝露年数とテロメラーゼ活性との間には負の関係が見られましたが、これは前述した、エストロゲンはテロメラーゼを活性化するという以前の報告(試験管内)と異なっているように思われます。しかし、本研究では、テロメラーゼ活性は閉経後数年以上経ってから測定されました。テロメラーゼ活性は、当然のことながら、エストロゲンが存在しているときは活性化されていますが、エストロゲンが存在しなくなれば低下します33)。そのことから、閉経後数年以上経ったときに測定されたテロメラーゼ活性は、内因性のエストロゲンが低下した時の状態を示しているために、当然低下しているものと考えられます。 エストロゲンを内因性ではなく、外因性に投与した時に、投与しない場合と比較してテロメアにどういう効果があるか検討されました34)。被験者は、55歳から69歳までの閉経後の女性で、5年以上ホルモン療法を受けているグループ(65人)と、閉経後ホルモン療法を受けていないグループ(65人)のテロメアの長さが比較検討されました。その結果、ホルモン療法を受けているグループは、ホルモン療法を受けていないグループに比べ、より長いテロメア長を持っていました。ホルモン療法を受けているグループは、ホルモン療法を受けていないグループに比べ、BMI、空腹時血糖値が有意に(統計的に)に低く、HDLコレステロールが有意に高く、運動頻度やビタミン摂取率が有意に高く、これらがテロメア長に影響している可能性が考えられましたので、これらの因子を調整して統計解析がなされた結果、テロメア長と関係があるのはホルモン療法のみでした。 以上のことから、女性ホルモン(エストロゲン)は、その抗酸化作用とテロメラーゼ活性化作用によりテロメア長を長く維持します。その結果、女性は男性に比べ老化や老化病にかかりにくく寿命が長いものと考えられました。しかし、女性ホルモン(エストロゲン)は、当然のことながら男性には投与することはできないので、男性は女性ホルモンの抗老化作用、老化病抑制作用、長寿命効果を享受することはできません。また、女性でも閉経後は女性ホルモンは激減するため、その効果を享受することはできません。その場合はホルモン療法(HRT)あるいはエストロゲン療法(ERT)がありますが、心血管系、乳がん、静脈血栓症など種々の副作用の問題からその使用法や使用期間などに制限があります35)。ではそのせっかくの良い効果は男性や閉経後女性は享受できないのでしょうか。それに対する答えはNO(一酸化窒素)にあります。エストロゲンのテロメラーゼ活性化作用30)、血管36)や骨37)に対する作用、(細胞)老化抑制作用30b)など、その健康効果の多くは一酸化窒素を介することが知られています。そのために、NOをアルギニンから生成する酵素、一酸化窒素合成酵素(NOS、特にeNOS)を活性化する成分(アルギニンなど)を使うことによってエストロゲンと同等以上の(NOの直接効果もありますので)抗老化、老化病抑制効果、寿命延長効果などが期待できます。また、アルギニンはアミノ酸ですので安全性が高く安心して摂取することができます。もちろん性ホルモン作用はありません。 ◎アルギニン(NO)とテロメラーゼの関係 テロメラーゼはNO(一酸化窒素)によって主にコントロールされていると考えられています38、39)。細胞の老化やテロメア長、テロメラーゼ活性がNOによってどういう影響があるかが検討されました40)。血管内皮細胞(ヒト臍帯静脈由来、HUVEC)は、細胞分裂させるたびに老化していき、それと共にテロメア長が短くなっていきました。また、テロメラーゼ活性は細胞分裂と共に低下しました。テロメラーゼ活性の低下は細胞老化の開始に先行していました。つまり、細胞は分裂するたびに少しづつテロメラーゼ活性が低下していき、それと共にテロメア長が短くなり、細胞老化が進むと考えられました。この細胞老化に対するNOの効果が検討されました。血管内皮細胞(HUVEC)はNO存在下で培養すると、細胞の老化は最大約50%抑制されました。また、老化の抑制と共にテロメラーゼ活性の低下およびテロメア長の短縮も抑制されました。一方、血管内皮細胞(HUVEC)をNOS(一酸化窒素合成酵素)阻害剤〔アルギニンからNOを合成する酵素(NOS)の働きを阻害してNOが合成されないようにする化合物〕と共に培養すると、テロメラーゼ活性は強力に抑制され、老化は促進されました。それに対し、血管内皮細胞(HUVEC)をNOと共に培養すると、テロメラーゼ活性は約3倍増加しました。すなわち、NOはテロメラーゼ活性をコントロールしているものと考えられました。なお、血管内皮細胞の老化は動脈硬化や老化の促進因子になると考えられています。 eNOS(血管内皮型一酸化窒素合成酵素)の活性化(NO生成の増加)がテロメラーゼ活性にどういう影響を示すかが検討されました41)。HEK293細胞(ヒト胎児腎細胞由来)またはHUVEC(ヒト臍帯静脈由来血管内皮細胞)にeNOSを遺伝子導入しますと、NOの生成は1.82倍に増加し、テロメラーゼ活性は2.24倍に増加しました。一方、細胞の老化はeNOSの導入によって抑制されました。糖尿病においては、動脈硬化のリスクが大幅に増加し、動脈硬化性疾患(心筋梗塞、脳梗塞、閉塞性動脈硬化症など)に罹りやすくなることが知られていますが、その原因は、高血糖によって血管内皮細胞が障害を受け、eNOSの活性が低下するためと考えられています(NOは抗動脈硬化因子です)。実際、HUVECを高濃度のグルコースに曝しますと、高濃度になるほどeNOSの発現レベルが減少しました。また、NOの生成はグルコースの濃度の増加と共に減少し、逆に活性酸素の生成量は増加しました。一方、高濃度のグルコースによって低下したNOの生成量は、アルギニンによって回復する傾向にありました。次いでアルギニンにシトルリンを加えると回復の程度は増加しました。さらにアルギニンとシトルリンに加え抗酸化剤(ビタミンC+ビタミンE)を同時に加えますと、NOの生成量はより増加し、ほぼ正常レベルまで回復しました。このことは、アルギニンとシトルリンと抗酸化剤(ビタミンC+ビタミンE)の間には相加効果あるいは相乗効果があるということを示しています。細胞老化に対する高濃度グルコースの影響を見てみますと、細胞(HUVEC)は、高濃度のグルコースによって老化が促進されました。また、テロメラーゼ活性は低下しました。一方、高濃度のグルコースによる細胞の老化は、アルギニンによって抑制される傾向にありました。次いでアルギニンに加えシトルリンを加えますと老化抑制の程度は増加しました。さらにアルギニンとシトルリンに加え抗酸化剤(ビタミンC+ビタミンE)を同時に加えますと、老化抑制の程度はより増加し、明らかに(統計的に有意に)老化は抑制されました。次に、細胞にeNOSを導入しますと高濃度のグルコースによる細胞の老化は抑制される傾向にありましたが、eNOSの活性化剤であるアルギニンを加えると老化抑制の程度はより増加しました。これにシトルリンを加えますと老化抑制の程度はさらに増加しました。次いで、これに抗酸化剤(ビタミンC+ビタミンE)を加えますと老化はさらに抑制され、統計的に有意に抑制されました。このように、細胞の老化に対しても、シトルリンと抗酸化剤はアルギニンの働きを相加的または相乗的に増強しました。 では、どうしてアルギニンとシトルリンと抗酸化剤を同時に加えると、アルギニンの働きが相加的または相乗的に増強されるのでしょうか。先ずシトルリンですが、二つの可能性があります。一つは、シトルリンは内皮細胞を含む種々の細胞においてアルギニンに変換されることが知られています42)。このことから、シトルリンを加えることでアルギニンの濃度が高くなったためと考えられます。もう一つの可能性はアルギナーゼが関係しています。アルギナーゼはアルギニンをオルニチンと尿素に分解する酵素ですが、内皮細胞などに発現しています43、44)。アルギナーゼは種々の因子によってその発現が促進されますが、内皮細胞においては、糖尿病(高血糖)、活性酸素、高血圧、酸化LDL(動脈硬化の原因物質の一つ)などによってアルギナーゼの発現が促進されます。このような場合に、アルギニンはアルギナーゼによって分解されるため、アルギニンの濃度は減少しNOの生成は低下します。一方、シトルリンはアルギナーゼを阻害し、アルギニンの分解を抑制します42、45)。このように、シトルリンは、これら二つの作用の一つまたは両作用によって細胞内のアルギニン濃度を高く保つと考えられます。 次に抗酸化剤について述べます。eNOSはアルギニンからNOを合成する酵素ですが、活性酸素によって容易にその活性が低下します。一方、抗酸化剤は活性酸素を消去し、eNOSの活性低下を抑制します。このようなメカニズムによって、アルギニンと抗酸化剤を同時に加えることによって、アルギニン単独よりもNOの生成が増強されると考えられます46、47、48)。また、抗酸化剤は、活性酸素を消去することで、活性酸素によるテロメラーゼ活性の減少やテロメアの短縮を抑制します。 以上まとめますと、アルギニンは、eNOSの働きでNOに変換され、これが細胞のテロメラーゼを活性化し、テロメアを長く保持することで老化を抑制したものと考えられました。また、アルギニンの働きは、シトルリンや抗酸化剤によって相加的または相乗的に増強されました。 1-1-3)アルギニン(NO)および他成分のテロメラーゼおよびテロメアに対する作用と老化および老化病抑制作用(まとめ) 次の図は、アルギニン(NO)のテロメラーゼ活性化作用と老化や老化病抑制作用との関係、また、シトルリンのアルギニンへの変換やアルギナーゼ抑制作用、抗酸化剤のeNOS活性化作用や老化および老化病抑制作用との関係を示しました。これらの作用により、アルギニン(NO)や抗酸化剤は老化や老化病を抑制することが期待できます。さらに、アルギニン(NO)とシトルリンと抗酸化剤を同時に摂取することでさらに強力に老化や老化病を抑制することが期待できます。寿命を延ばし、老化や老化病を抑制するといわれている多くの生体成分や天然成分、あるいはライフスタイルがテロメラーゼ活性化作用や保護作用、テロメア保護作用を示すことが報告されていますが、その作用にはそれらの抗酸化作用やNOを介する作用が働いているものと考えられます。 図.アルギニン(NO)および他成分のテロメラーゼおよびテロメアに対する作用と老化および老化病抑制作用との関係 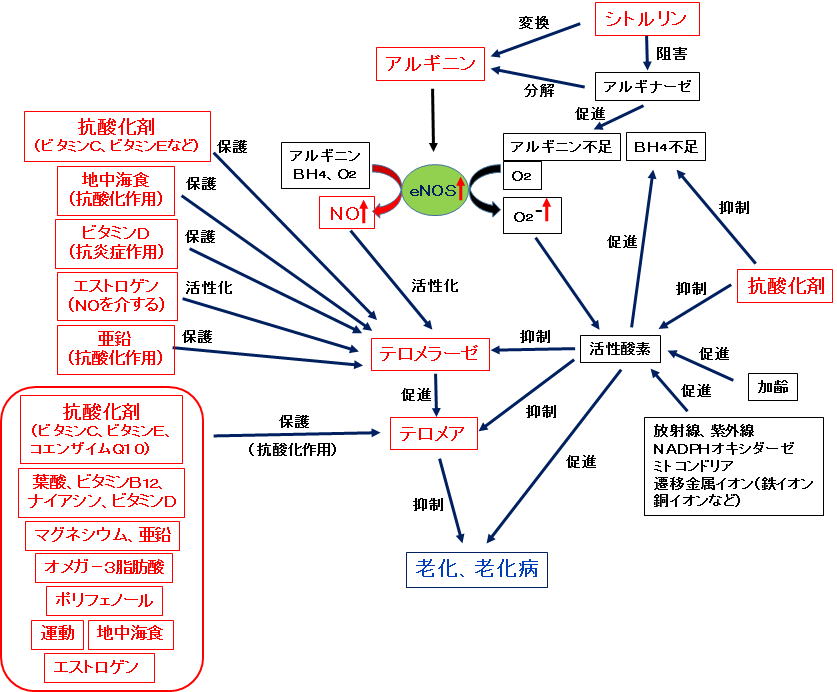 アルギニンからeNOS(血管内皮型一酸化窒素合成酵素)の働きで生成したNO(一酸化窒素)は、テロメラーゼを活性化しテロメアを長くします。テロメアを長くすることで老化や老化病が抑制され、寿命が延長することが期待できます。シトルリンは体内でアルギニンに変換されアルギニンの供給源となります。また、シトルリンは、アルギニンを分解しアルギニン不足をもたらすアルギナーゼの働きを阻害します。一方、加齢、放射線、紫外線、NADPHオキシダーゼ、ミトコンドリア、遷移金属(鉄イオン、銅イオンなど)などにより生成した活性酸素は、eNOSの正常な働きに必要なBH4(テトラヒドロバイオプテリン)を酸化し減少させます。BH4やアルギニンの不足は、eNOSの正常な働き(アルギニンからNOを生成する)を阻害し、NOを生成する代わりに活性酸素(スーパーオキシド、O2-)を生成します(eNOSアンカップリング)。そのため、抗酸化剤(ビタミンCなど)はBH4の減少を防ぎ、eNOSを活性化し、NOの生成を促進します。つまり、アルギニンと抗酸化剤は相乗的にeNOSを活性化しNOの生成を促進します。また、活性酸素はテロメラーゼやテロメアを抑制し、老化や老化病を促進しますが、抗酸化剤は活性酸素の害から体を守り、老化や老化病を抑制します。このように、アルギニン単独でも老化や老化病を強力に抑制しますが、シトルリンや抗酸化剤を同時に摂取することでより強力に老化や老化病を抑制し、寿命(勿論健康寿命も)を延長するものと考えられます。すなわち、アルギニンは、NOのテロメラーゼ活性化作用によってテロメア長を維持し、老化や老化病(肥満、メタボリックシンドローム、高血圧、糖尿病、動脈硬化、心血管病、骨粗鬆症、認知症、がんなど)を抑制し、寿命を延長することが期待できます。 一方、種々の生体成分や天然成分やライフスタイルがテロメラーゼを活性化(保護)したり(抗酸化剤、地中海食、ビタミンD,エストロゲン、亜鉛など)、テロメアを保護してその短縮を抑制したり〔抗酸化剤、ビタミン類(葉酸、ビタミンB12、ナイアシン、ビタミンDなど)、ミネラル(マグネシウム、亜鉛など)、オメガ―3脂肪酸、ポリフェノール、運動、地中海食、エストロゲンなど〕することが報告されていますが、それらの働きはそれら成分やライフスタイルによる抗酸化作用やNOを介する作用が主に関係しているものと考えられます。 (文献、資料) 1)「老化・寿命のサイエンス」(実験医学増刊、2013)。 2)「ハーパー・生化学」(原書29版)(丸善出版、平成25年)。 3)「アンチエイジング医学の基礎と臨床」(日本抗加齢医学会。2011年)。 4)「健康寿命を伸ばす!アンチエイジングへの取り組み」(東洋出版、2014年)。 5)「細胞増殖の仕組み-細胞周期、癌遺伝子、細胞老化-」(薬学雑誌、126、1087(2006))。 6)"Association between telomere length in blood and mortality in people aged 60 years or older" Lancet, 361, 393 (2003). 7)"Association Between Higher Plasma Lutein, Zeaxanthin, and Vitamin C Concentrations and Longer Telomere Length: Results of the Austrian Stroke Prevention Study" J Am Geriatr Soc, 62, 222 (2014). 8)"Multivitamin use and telomere length in women" Am J Clin Nutr, 89, 1857 (2009). 9)"Diet, nutrition and telomere length" Journal of Nutritional Biochemistry, 22, 895 (2011). 10)"Mortality in randomized trials of antioxidant supplements for primary and secondary prevention: systematic review and meta-analysisi" JAMA, 297, 842 (2007). 11)国立健康・栄養研究所の「健康食品」の安全性・有効性情報の『ビタミンA(レチノール)』の項を参照ください。 12)国立健康・栄養研究所の「健康食品」の安全性・有効性情報の『カロテン』の項を参照ください。 13)"Coenzyme Q10 prevents accelerated cardiac aging in a rat model of poor maternal nutrition and accelerated postnatal growth" Molecular Metabolism, 2, 480 (2013). 14)"The association Between Physical Activity in Leisure Time and Leukocyte Telomere Length" Arch Intern. Med, 168, 154 (2008). 15)「活性酸素の本当の姿」(有限会社ナップ、2014年)。 16)"Effect of Different Intensities of Exercise on Endothelium-Dependent Vasodilation in Humans - Role of Endothelium-Dependent Nitric Oxide and Oxidative Stress" Circulation, 108, 530 (2003). 17)"Antioxidants prevent health-promoting effects of physical exercise in humans" Prc Natl Acad Sci USA, 106, 8665 (2009). 18)"Meta-Analysis: High-Dosage Vitamin E Supplementation May Increase All-Cause Mortality" Ann Intern Med, 142, 37 (2005). 19)"Telomerase reactivation reverses tissue degeneration in aged telomerase deficient mice" Nature, 469, 102 (2011). 20)"Mediterranean Diet, Lifestyle Factors, and 10-Year Mortality in Elderly European Men and Women" JAMA, 292, 1433 (2004). 21)"Mediterranean Diet, Telomere Maintenance and Health Status among Elderly" PLoS One, 8, e62781 (2013). 22)WHO資料。総務省統計局。 23)"Study Finds DNA Length Can Predict Life Expectancy" (Intermountain Medical Center, USA, 2013)など。 24)"Adherence to a Mediterranean Diet and Survival in a Greek Population" N Engl J Med, 348, 2599 (2003). 25)”健康日本21(アルコール)”(厚生労働省)。 26)"Vitamin D and the risk of dementia and Alzheimer disease" Neurology, 83, 920 (2014). 27)"Higher serum vitamin D concentrations are associated with longer leukocyte telomere length in women" Am J Clin Nutr, 86, 1420 (2007). 28)"Increased Telomerase Activity and Vitamin D Supplementation in Overweight African Americans" Int J Obes (Lond), 36, 805 (2012). 29)"Sex differences in telomeres and lifespan" Aging Cell, 10, 913 (2011). 30a)"Estrogen Receptor-α and Endothelial Nitric Oxide Synthase Nuclear Complex Regulates Transcription of Human Telomerase" Circ Res, 103, 34 (2008). 30b)"Endothelial cellular senescence is inhibited by nitric oxide: Implications in atherosclerosis associated with menopause and diabetes" Prc Natl Acad Sci USA, 103, 17018 (2006). 31)「エストロゲンと血管」 日本生殖内分泌学会雑誌、18、11(2013)。「閉経後脂質異常症」 日産婦誌、61、N-520(2009)など。 32)"Greater endogeneous estrogen exposure is associated with the telomere maintenance in postmenopausal women at risk for cognitive decline" Brain Res, 16, 1379 (2011). 33)"Estrogen deficiency reversibly induces telomere shortening in mouse granulosa cells and ovarian aging in vivo" Protein Cell, 2, 333 (2011). 34)"Effect of Long-Term Hormone Therapy on Telomere Length in Postmenopausal Women" Yonsei Medical Journal, 46, 471 (2005). 35)「ホルモン補充療法ガイドライン2012年度版解説」 日産婦誌、65、N-49(2013)。「HRTは何時まで続けることが可能か」 日産婦誌、63、N-155(2011)。 36)"Mechanism of Cerebrovascular Protection: Estrogen, Inflammation and Mitochondria" Acta Physiol (Oxf), 203, 149 (2011). 37)"Nitric oxide as a mediator of estrogen effects in osteocytes" Vitam Horm, 96, 247 (2014). 38)"The telomerase tale in vascular aging: regulation by estrogens and nitric oxide signaling" J Appl Physiol, 106,333 (2009). 39)"Mechanisms involved in the aging-induced vascular dysfunction" Frontiers in Physiology, 3, 1 (2012). 40)"Nitric Oxide Activates Telomerase and Delays Endothelial Cell Senescence" Circ Res, 87, 540 (2000). 41)"Endothelial cellular senescence is inhibited by nitric oxide: Implications in atherosclerosis associated with menopause and diabetes" Prc Natl Acad Sci USA, 103, 17018 (2006). 42)"Therapeutic Use of Citrulline in Cardiovascular Disease", Cardiovascular Drug Reviews, 24, 275 (2006). 43)"Arginase as a potential target in the treatment of cardiovascular disease: reversal of arginine steal?", Cardiovascular Research, 98, 334 (2013). 44)"Arginases and Arginine Deficiency Syndromes", Curr Opin Clin Nutr Metab Care, 15, 64 (2012). 45)"Diabetes-induced Coronary Vascular Dysfunction Involves Increased Arginase Activity", Circ Res, 102, 95 (2008). 46)"Effects of vitamin C on intracoronary L-arginine dependent coronary vasodilatation in patients with stable angina", Heart, 91, 1319 (2004). 47)"Beneficial effects of antioxidants and L-arginine on oxidation-sensitive gene expression and endothelial NO synthase activity at sites of disturbed shear stress", Proc Natl Acad Sci USA, 100, 1420 (2003). 48)"Tetrahydrobiopterin, L-Arginine and Vitamin C Act Synergistically to Decrease Oxidant Stress and Increase Nitric Oxide That Increases Blood Flow Recovery after Hindlimb Ischemia in the Rat", Mol Med, 18, 1221 (2012).
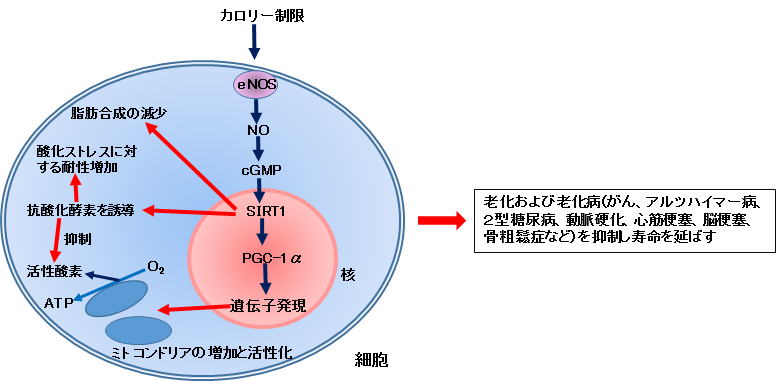
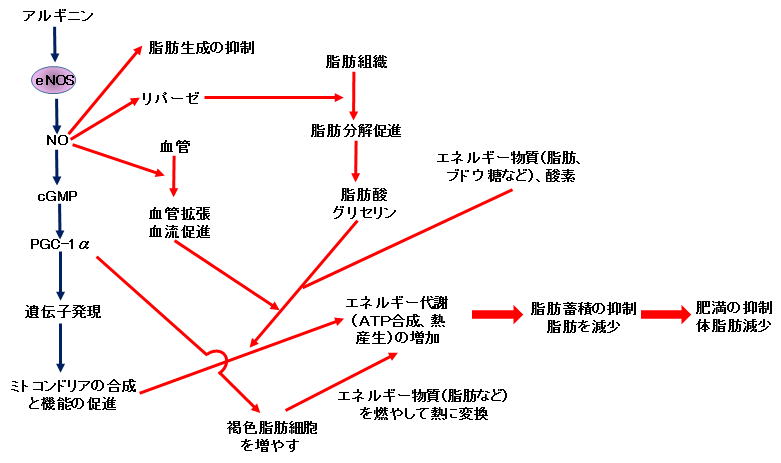
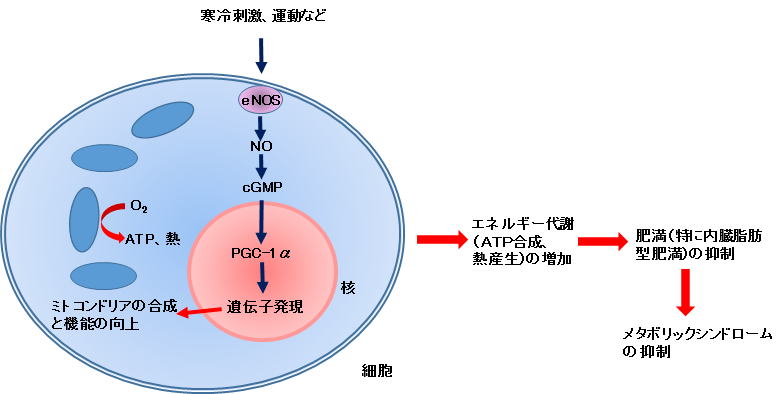
1-2)長寿遺伝子説 現在、多くの生物で共通して寿命を延長する唯一の方法はカロリー制限です。原生動物、ミジンコ、クモ、魚、マウス、ラットなど幅広い動物種で摂取カロリーを制限すると共通して寿命が1.4倍から1.9倍に延長することが明らかとなりました1、2)。ラットの場合は60~70%カロリー制限を行うと寿命は1.4倍延長しました。サルや人でもその可能性が示唆されています。カロリー制限を受けているマウスやラットでは通常食のマウスやラットに比べ小さく痩せており、脂肪蓄積量も少ないことが示されています。また、主要な臓器が小さくなります。さらに、より活発に動き、見た目を若く保ち、老化や老化病が抑制されますが、低温に対する抵抗力が弱くなります。また、カロリー制限を始める時期や行っている期間が寿命延長の効果に影響を与えます。 しかし、カロリー制限を人に応用するには多くの問題点があります。実験動物は通常ほとんど無菌状態で飼育されており、人の生活条件とは異なります。また、カロリー制限は成長に影響するため、成長期にそれを行うのは好ましくありません。実際には目立った老化が始まる30代後半から40代くらいで始めるのが望ましいと考えられます。一方、動物実験で行われたようなかなり厳しいカロリー制限は現代人には到底実施し難いように思われ、また例え出来ても長続きしないと考えられます。これらのことから、一般の人が寿命を延長するほどのカロリー制限を半生でも続けられるとはとても思えません。ということで、カロリー制限と同様なメカニズムで寿命の延長ができ、手軽に、そして長期間の摂取にも問題のない安全性の高い物質の探索が進められ、いくつかの物質が候補に上げられてきました。 カロリー制限による寿命延長や老化抑制には様々な因子が関与していることが報告されていますが、その中で主要な因子としてサーチュインが知られています。サーチュインはサーチュイン遺伝子(長寿遺伝子とも呼ばれています)の活性化により合成されるタンパク質で、色々なメディアでも広く取り上げられるようになったため、一般の人々にも広く知られる存在になってきました2)。そのため、サーチュインを活性化する物質が老化を抑制し長寿をもたらすのではないかと熱い期待が寄せられています。 サーチュインは様々な働きを示しますが、中でも重要なのはPGC-1αを活性化し、ミトコンドリアを活性化することです。サーチュイン(SIRT1)の働きを遺伝子導入法により高めたマウスでは、カロリー制限で見られるのと同様な現象が見られました。一方、遺伝子欠損法でSIRT1を欠損させたマウスではカロリー制限による運動機能改善や寿命延長が見られなくなりました。これらのことから、サーチュイン(SIRT1)は、カロリー制限による老化抑制や寿命延長などの効果をもたらす主要な因子と考えられました。 では、サーチュイン遺伝子(長寿遺伝子)を活性化し、ミトコンドリアを活性化することが、なぜ老化や老化病の抑制、あるいは寿命延長に結びつくのでしょうか。それについて少し詳しく述べたいと思います。 (文献、資料) 1)「アンチエイジング医学の基礎と臨床」(日本抗加齢医学会。2011年)。 2)「老化・寿命のサイエンス」(実験医学増刊、2013)。 1-2-1)ミトコンドリアとは 電気は私たちが生活していくうえでなくてはならないもので、もし電気が不足したり供給されなくなると私たちの生活は大変不自由になり、また都市機能そのものが破たんしてしまいます。 それと同様に私たちが生きていくためにはエネルギーが必要です。動いているとき、運動しているとき、また、寝ているときでさえ私たちの体は常にエネルギーを必要とします。私たちの体がエネルギーとして使っているものはATPといわれる高エネルギー化学物質です。もし私たちの体の中でATPが作られなくなったらすぐに死んでしまうでしょう。またその供給量が少なくなったら体がうまく働かなくなって元気がなくなったり、疲れやすくなったり、代謝がうまくいかなくなったり、老化が進んだり、色んな病気になってしまうでしょう。 ではエネルギーの元であるATPはどこで作られているのでしょう。そのほとんど(80~90%)はミトコンドリアというところで作られています。ミトコンドリアという言葉は最近書物やテレビなどでよく取り上げられていますのでご存知の方も多いのではないでしょうか1)。〔最近では、ミトコンドリアが「ためしてガッテン」で取り上げられました(2015年8月26日放送)(さわりの部分だけですが参考にはなると思います)〕。 ミトコンドリアというのはほとんどの細胞の中にある小器官のひとつで、その量は消費されるエネルギーと関係があり、エネルギーをたくさん使う部位(組織や臓器)の細胞にはミトコンドリアの量も多く存在します。体内のエネルギーの4割を消費する骨格筋ではたくさんのミトコンドリアが見られます。特に心臓には臓器の中で一番多くのミトコンドリアが存在します。これは心臓がいつも動いているからでエネルギーを最も多く使うからです。このようにミトコンドリアは細胞に必要なエネルギーのほとんどを生成するために、細胞内の”発電所”と呼ばれています。 実際の発電所(火力)では、燃料として主に石炭、石油、天然ガスを使いますが、ミトコンドリアでは食物として摂取した脂肪、炭水化物、タンパク質が燃料となります。実際にはそれらが消化吸収された脂肪酸、グリセロール、グルコースなど(糖類)、アミノ酸が燃料となります。それらが利用されやすい形に変えられて、ミトコンドリア内で酸素と反応してエネリギーであるATPを生成します。これはミトコンドリアから細胞内に放出されてエネルギーとして使われます。上に述べましたように多くのエネルギ-を必要とする細胞には多くのミトコンドリアが存在します。 一方、ミトコンドリアで食物の酸化によって生じたエネルギーの一部は熱として放出されます。これは体温の維持に使われます。熱産生に特化した細胞に褐色脂肪があります。褐色脂肪組織は特に体内で熱発生が必要な時〔寒冷下におかれた時など(非ふるえ産熱)〕活発に活動します。この組織には特にミトコンドリアの量が多いことが知られています。ここでは特にグルコースと脂肪酸の両者の酸化が活発です。褐色脂肪組織ではこれらの酸化によって得られたエネルギーはほとんどが熱になり、ATPの生成はわずかにすぎません。興味あることに肥満の人では褐色脂肪組織が減少しているかほとんど無いといわれています。 このように私たちの体に必要なエネルギー(ATP)のほとんどはミトコンドリアで生成されることが分かりました。ではこのミトコンドリアに異常がおこったり、数が少なくなったらどうなるでしょうか。その場合、ミトコンドリアの働きが悪くなったり不足したりして、体に必要なエネルギーは不足し、様々な影響が出てきます。例えば、少し~中程度に不足した場合は、疲れやすくなったり、疲労が抜けにくくなったり、頑張りが効かなくなったり、太りやすくなったり(食べたものが消費されにくくなって脂肪として蓄積されやすくなります)、老化が進んだり(代謝が悪くなるため)すると考えられます。それが持続すると老化病、肥満、糖尿病などを引き起こす原因となり、寿命も短くなると考えられます。また最近では、ミトコンドリアの異常とがんの転移やアルツハイマー病が関係あることが言われています。実際、老化によってミトコンドリアの数や機能が低下することが知られています。 (文献) 1)例えば、古くは「パラサイト・イヴ」(瀬名秀明のデビュー作となったホラー小説)、最近では「ミトコンドリアの新常識」(NHKサイエンスゼロ、2011年)、「ウェスト20cm減、体重15kg減!ミトコンドリア・ダイエット」(内藤眞禮生、2012年)など。
 2.アルギニンの寿命延長、老化および老化病の予防・改善作用 2.アルギニンの寿命延長、老化および老化病の予防・改善作用
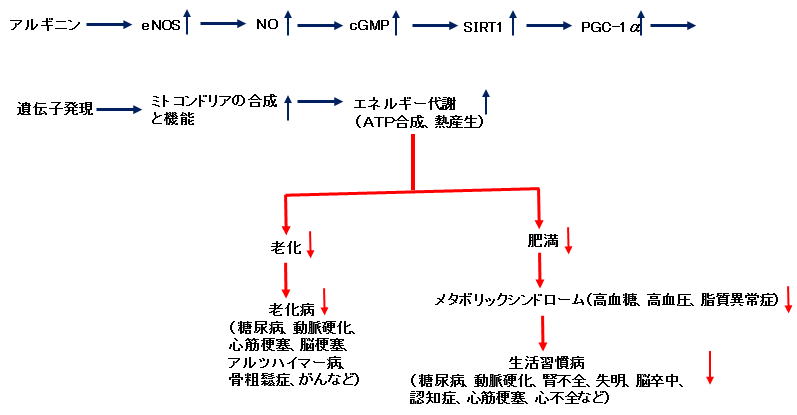
図.アルギニン(NO)の寿命延長、抗老化および老化病抑制のメカニズム 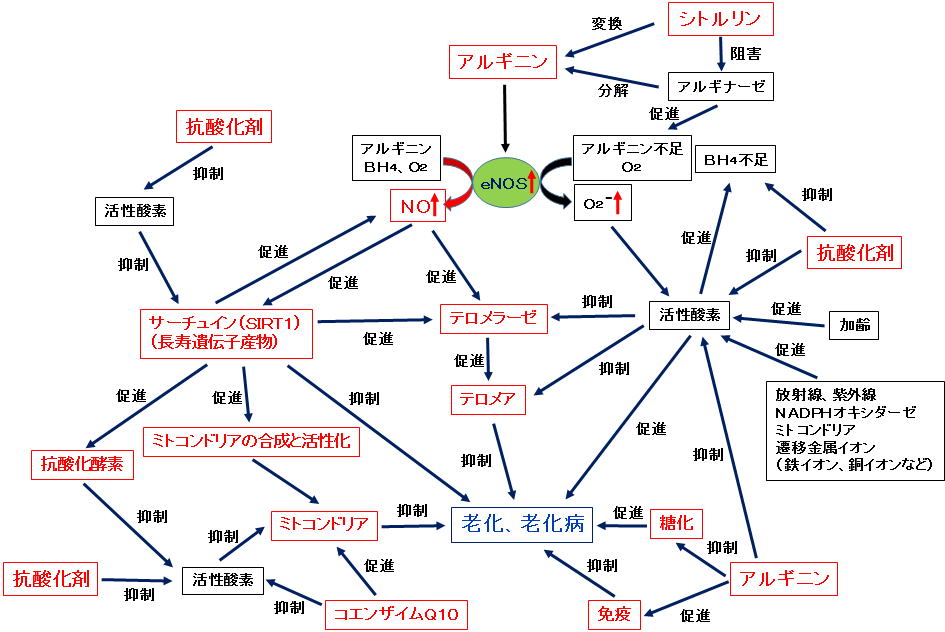 アルギニンからeNOS(血管内皮型一酸化窒素合成酵素)の働きで生成したNO(一酸化窒素)は、テロメラーゼを活性化しテロメアを長くします。テロメアを長くすることで老化や老化病が抑制され、寿命が延長することが期待できます。また、NOは、長寿遺伝子からつくられるタンパク質のサーチュイン(SIRT1)の生成を促進します。サーチュインは逆にeNOSを活性化します(ポジティブフィードバック)。サーチュインを活性化することで老化や老化病が抑制され、寿命の延長が期待できます。サーチュインは、抗酸化酵素の生成を促進して酸化ストレス(活性酸素が過剰な状態)を抑制して老化や老化病を抑制します。また、サーチュインはミトコンドリアの生成と活性化を促進し、老化や老化病を抑制します。さらにサーチュインはテロメラーゼも活性化します。すなわち、アルギニンは、NOのテロメラーゼ活性化作用とサーチュイン活性化作用によって、老化や老化病(肥満、メタボリックシンドローム、高血圧、糖尿病、動脈硬化、心血管病、骨粗鬆症、認知症、がんなど)を抑制し、寿命を延長することが期待できます。 一方、加齢、放射線、紫外線、NADPHオキシダーゼ、ミトコンドリア、遷移金属(鉄イオン、銅イオンなど)などにより生成した活性酸素は、eNOSの正常な働きに必要なBH4(テトラヒドロバイオプテリン)を酸化し減少させます。BH4の不足によって、eNOSはNOを生成する代わりに活性酸素(スーパーオキシド、O2-)を生成します(eNOSアンカップリング)。そのため、抗酸化剤(ビタミンCなど)は活性酸素を消去し、BH4の減少を防ぎ、NOの生成を促進します。つまり、アルギニンと抗酸化剤は相乗的にeNOSを活性化しNOの生成を促進します。また、活性酸素はテロメラーゼ、テロメア、サーチュイン、ミトコンドリアを抑制し、老化や老化病を促進しますが、抗酸化剤の強化や抗酸化酵素を活性化することで、活性酸素の害から体を守り、老化や老化病を抑制します。このように、アルギニン単独でも老化や老化病を強力に抑制しますが、抗酸化剤を同時に摂取することでより強力に老化や老化病を抑制し、寿命(勿論健康寿命も)を延長するものと考えられます。また、、ミトコンドリアの働き(エネルギー産生など)にはコエンザイムQ10が補酵素として必須ですが、コエンザイムQ10は加齢とともに体内の量が減少すると言われています1)。折角アルギニンによってミトコンドリアの生成を促進してもコエンザイムQ10が不足していてはミトコンドリアは十分に働くことはできません。そのため、アルギニンと抗酸化剤だけでなく、コエンザイムQ10を共に摂取することでより強く老化や老化病を抑制することが期待できます。なお、コエンザイムQ10は抗酸化活性を持っています。コエンザイムQ10はビタミンC、ビタミンEと共に体内で強力な抗酸化ネットワークを形成しているために、体内の抗酸化能をより強化するためにも、ビタミンC、ビタミンEと共にコエンザイムQ10を摂取することが望ましいと考えられます1)。 他方、老化、老化病(メタボリックシンドローム、糖尿病、高血圧、動脈硬化、心筋梗塞、脳卒中、糖尿病性血管障害、心不全、末梢血管障害、ED、がんなど)、肺動脈高血圧症、喘息、肝障害、妊娠高血圧症候群、感染症などにおいて、あるいはアルギニンの長期摂取(例えば3ヶ月程度以上)や大量摂取(摂取量が多いほど)において、アルギナーゼという酵素が活性化されます。アルギナーゼは体内の至る所に存在しアルギニンを分解しますので、特に上記のようにアルギナーゼが活性化される場合、アルギニンの体内濃度が減少したり枯渇します。そのような場合、原料(アルギニン)不足により、eNOSはNOを生成する代わりに活性酸素(スーパーオキシド、O2-)を生成します(eNOSアンカップリング)。そのため、アルギナーゼ活性が高い場合、折角アルギニンを摂取しても、アルギニンは効果を示さないか、逆に生成した活性酸素によって体は障害を受けることになります。なお、この場合、アルギニンの効果が弱かったり示されないからといって、アルギニンの摂取量を増やしても、アルギナーゼはかえって活性化されるため逆効果になります。従って、アルギニンを老化や老化病抑制のために長期間(特に3ヶ月程度以上)に渡って摂取する場合、アルギナーゼ対策は必須のこととなります。シトルリンは、安全に長期間摂取できるアルギナーゼ阻害剤として近年大変注目されています。また、シトルリンは、体内でアルギニンに変換され、アルギニンとしても効果を発揮しますので、まさに一石二鳥となります。 このように、アルギニン+シトルリン+抗酸化剤の組み合わせは、長寿、抗老化、老化病抑制のための、現在最高のスーパーアンチエイジングサプリと考えられますが、それらの成分の比率や、抗酸化剤に何を組み合わせるかなどについては、最新のデータをもとに、最高のものにしなければなりません。 これについては詳しくは「アルギニンの欠点を克服し、超強力・超持続を目指した、進化型「スーパーアルギニンサプリメント」の開発の試み〚詳細編〛」または「アルギニンの欠点を克服し、超強力・超持続を目指した、進化型「スーパーアルギニンサプリメント」の開発の試み〚概要編〛」をご参照ください。 (文献、資料) 1)”コエンザイムQ10への期待” New Food Industry, 44, 1 (2002)。 |
 |
 |
| 3.お知らせ(ホームページ責任者、参考図書) |
【ホームページ責任者】 古賀 弘 Eメール:kogahrs555@nifty.com 健康コンサルタント 医薬品・健康食品研究開発コンサルタント 薬学博士(東京大学) 日本抗加齢医学会正会員 ◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆ 【参考図書】 「アルギニン」についてもっとお知りになりたい方には次の本(拙著)をお薦めします。本書は本邦最初で唯一の一般向けアルギニン参考書です。 本書のご購入ご希望の方はインターネット書店(Amazon.co.jpまたは紀伊国屋書店)または全国の書店でお買い求め下さい。 『超アミノ酸健康革命-21世紀のサプリメント「アルギニン」のすべて』(古賀 弘著、今日の話題社、1,575円(税込)) |
 |
 |
 |
 リンク集 リンク集 |
| ためしてガッテン |
『ためしてガッテン』のホームページです。最新の健康情報(糖尿病、動脈硬化など)について分かりやすく解説してあります。過去の放送テーマを見ることができます(キーワード検索もできます)。
|
 |